| Autor |
Mensaje |
sebasgm
Moderador
Edad: 38
Registrado: 07 Jul 2006
Mensajes: 2434
Ubicación: Parque Chacabuco
Carrera: Electrónica


|
|
bueno, aquí estoy de nuevo. Buscando si alguien había preguntadoesto ya, me encontré con una duda mia de un dia antes de rendir en marzo de este año (obviamente no aprobé), y curiosamente la duda era sobre lo mismo pero esa vez no tuve suerte, nadie puedo ayudarme, asi que acá voy de nuevo:
¿Alguien puede detallarme las ecuaciones del método cal soda correctamente y explicar bien cómo actuán?
Entiendo que a priori es medio trivial ver como actuan una vez que vas viendo qué hace cada una, pero creo que hay algo que no estoy viendo proque no me resulta intuitivo, no tengo bien copiadas las fórmulas, y no encuentro ni en internet ni en los libros que tengo, buen material (incluyendo un link que habia dejado Artemisa y que ahora no me anda).
Se los agradeceria porque este tema siempre me traba, y seria bueno despejar la duda.
Gracias.
|
|
|
|
_________________

"Por un foro más ordenado" "Cómo buscar en el Foro" "Información para ingresantes" "El wiki te espera"
|
|
   |
      |
 |
gira
Nivel 9

Edad: 36
Registrado: 13 Ago 2007
Mensajes: 2166
Carrera: Industrial


|
|
Hola sebas,
mira en mi cátedra ( boeykens, para industriales) del cuatri pasado nos subian todos los apuntes de cada tema y un resumen teorico de cada TP en un grupo yahoo. Yo sé que esos apuntes estan fotocopiados y andan dando vuelta en algún lado de la facultad, nose si fotocopiadroa o publicaciones o lo que sea, lo cierto es que yo tenia compañeros que ya tenían esos apuntes desde ppio del cuatrimestre y nose bien de donde los habrán sacado. En fin, nose si en esos apuntes esta lo de los Tps y nose si todo sirve para la quimica que ven ustedes, pero bueno te paso lo que tengo sobre el "metodo cal-soda" en los apuntes, (si necesitas apuntes de otros temas avisame):
Ablandamiento por el método de la cal-soda
Un método muy usado en la industria para ablandar agua dura es el de la cal soda. Se basa en la obtención de compuestos insolubles de calcio y magnesio usando cal (hidróxido de calcio) y soda (carbonato de sodio). De los compuestos de calcio, el más insoluble es el carbonato de calcio y de los de magnesio, el hidróxido de magnesio.
El bicarbonato de calcio, que constituye dureza temporaria, puede convertirse en carbonato tratándolo con un hidróxido. El hidróxido más barato es el de calcio (cal apagada). La dureza temporaria debida al calcio se elimina entonces con cal:
![[ce]Ca(HCO3)2 + Ca(OH)2 -> CaCO3(s) + H2O[/ce] [ce]Ca(HCO3)2 + Ca(OH)2 -> CaCO3(s) + H2O[/ce]](images/latex/5bb297b03e7d883c1e5bcd17e235945576cf0145_0.png)
La dureza debida al magnesio, tanto la temporaria como la permanente, se puede eliminar con cal:
Dureza temporaria: ![[ce]Mg(HCO3)2 + Ca(OH)2 -> Mg(OH)2(s) + CaCO3(s) + H2O[/ce] [ce]Mg(HCO3)2 + Ca(OH)2 -> Mg(OH)2(s) + CaCO3(s) + H2O[/ce]](images/latex/038dd1cd0b0250e6cbafee14cf151eff7a9f0ff7_0.png)
Dureza permanente: ![[ce]MgCl2 + Ca(OH)2 -> Mg(OH)2(s) + CaCl2(s) [/ce] [ce]MgCl2 + Ca(OH)2 -> Mg(OH)2(s) + CaCl2(s) [/ce]](images/latex/4b008606d392049c426297a6c4d39d8b8b507a5d_0.png)
Como se puede observar, al eliminar con cal dureza permanente debida al magnesio, se genera dureza permanente debida al calcio. La dureza permanente debida al calcio se elimina tratándola con carbonato de sodio:
![[ce]CaCl2 + Na2CO3 -> CaCO3(s) + NaCl[/ce] [ce]CaCl2 + Na2CO3 -> CaCO3(s) + NaCl[/ce]](images/latex/6d41a9b7882a407a8fd9588abc84a2f0999da5e6_0.png)
Cuando se utiliza este método para eliminar dureza en una industria, se mide la dureza total y se agrega en primera instancia cal suficiente para eliminarla y el doble de soda por si existiera magnesio. Luego se debe neutralizar el pH.
\MOD (4WD): Paso a CE 
|
|
|
|
_________________
- Material de ing. industrial en Skydrive
- Libros digitalizados de ing. industrial
- Planificaciones de materias industriales
- LaTeX en el Foro para todos
- Introducción a LaTeX
- Editor en línea de ecuaciones LateX
- El Rincón del Rock Progresivo
Cuanto más complicada parece una situación, más simple es la solución. Eliyahu Goldratt
|
|
   |
     |
 |
Amintoros
Nivel 8

Registrado: 20 Mar 2008
Mensajes: 533
Carrera: Química


|
|
Gira ya lo explicó, pero por las dudas acá te dejo el enunciado del trabajo práctico que lo químicos hacemos en 63.13, están brevemente explicadas las reacciones en las que se basa el método (página cuatro): Aguas
Si aún no alcanza, chiflá de nuevo 
|
|
|
|
|
|
 |
    |
 |
sebasgm
Moderador
Edad: 38
Registrado: 07 Jul 2006
Mensajes: 2434
Ubicación: Parque Chacabuco
Carrera: Electrónica


|
|
   |
      |
 |
altermaster
Nivel 6
Edad: 34
Registrado: 05 Sep 2009
Mensajes: 278
Carrera: Informática


|
|
creo q en esta 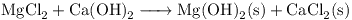
CaCl2 esta en estado (ac)
|
|
|
|
_________________
....
|
|
   |
    |
 |
altermaster
Nivel 6
Edad: 34
Registrado: 05 Sep 2009
Mensajes: 278
Carrera: Informática


|
|
| si o si hay que hacer dos pasos para la dureza permanente del Mg????
|
|
|
|
_________________
....
|
|
   |
    |
 |
La gallina Pipa
Nivel 8

Edad: 84
Registrado: 16 Jul 2010
Mensajes: 611
Ubicación: Calle Falsa 123
Carrera: No especificada


|
|
| altermaster escribió:
|
creo q en esta 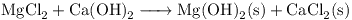
CaCl2 esta en estado (ac)
|
El cloruro de calcio es una sal soluble; asi que sí, se encuentra disociado en la solución acuosa.
| altermaster escribió:
|
|
si o si hay que hacer dos pasos para la dureza permanente del Mg????
|
En el método cal-soda sí: un paso para sacar la dureza permanente del Mg y otro para sacar la dureza permanente del Ca que se forma en la etapa anterior.
|
|
|
|
_________________
Nosotros... Chat FIUBA!
|
|
   |
     |
 |
altermaster
Nivel 6
Edad: 34
Registrado: 05 Sep 2009
Mensajes: 278
Carrera: Informática


|
|
si tengo agua con CaSO4 ,que da asi?=CaSO4 + Na2CO3 → CaCO3 + Na2SO4
?¡?¡
|
|
|
|
_________________
....
|
|
   |
    |
 |
La gallina Pipa
Nivel 8

Edad: 84
Registrado: 16 Jul 2010
Mensajes: 611
Ubicación: Calle Falsa 123
Carrera: No especificada


|
|
| altermaster escribió:
|
si tengo agua con CaSO4 ,que da asi?=CaSO4 + Na2CO3 → CaCO3 + Na2SO4
?¡?¡
|
Sí. 
|
|
|
|
_________________
Nosotros... Chat FIUBA!
|
|
   |
     |
 |
EZEQUIEL1214
Nivel 2
Registrado: 21 Mar 2010
Mensajes: 5


|
|
| gira escribió:
|
Hola sebas,
mira en mi cátedra ( boeykens, para industriales) del cuatri pasado nos subian todos los apuntes de cada tema y un resumen teorico de cada TP en un grupo yahoo. Yo sé que esos apuntes estan fotocopiados y andan dando vuelta en algún lado de la facultad, nose si fotocopiadroa o publicaciones o lo que sea, lo cierto es que yo tenia compañeros que ya tenían esos apuntes desde ppio del cuatrimestre y nose bien de donde los habrán sacado. En fin, nose si en esos apuntes esta lo de los Tps y nose si todo sirve para la quimica que ven ustedes, pero bueno te paso lo que tengo sobre el "metodo cal-soda" en los apuntes, (si necesitas apuntes de otros temas avisame):
Ablandamiento por el método de la cal-soda
Un método muy usado en la industria para ablandar agua dura es el de la cal soda. Se basa en la obtención de compuestos insolubles de calcio y magnesio usando cal (hidróxido de calcio) y soda (carbonato de sodio). De los compuestos de calcio, el más insoluble es el carbonato de calcio y de los de magnesio, el hidróxido de magnesio.
El bicarbonato de calcio, que constituye dureza temporaria, puede convertirse en carbonato tratándolo con un hidróxido. El hidróxido más barato es el de calcio (cal apagada). La dureza temporaria debida al calcio se elimina entonces con cal:
![[ce]Ca(HCO3)2 + Ca(OH)2 -> CaCO3(s) + H2O[/ce] [ce]Ca(HCO3)2 + Ca(OH)2 -> CaCO3(s) + H2O[/ce]](images/latex/5bb297b03e7d883c1e5bcd17e235945576cf0145_0.png)
La dureza debida al magnesio, tanto la temporaria como la permanente, se puede eliminar con cal:
Dureza temporaria: ![[ce]Mg(HCO3)2 + Ca(OH)2 -> Mg(OH)2(s) + CaCO3(s) + H2O[/ce] [ce]Mg(HCO3)2 + Ca(OH)2 -> Mg(OH)2(s) + CaCO3(s) + H2O[/ce]](images/latex/038dd1cd0b0250e6cbafee14cf151eff7a9f0ff7_0.png)
Dureza permanente: ![[ce]MgCl2 + Ca(OH)2 -> Mg(OH)2(s) + CaCl2(s) [/ce] [ce]MgCl2 + Ca(OH)2 -> Mg(OH)2(s) + CaCl2(s) [/ce]](images/latex/4b008606d392049c426297a6c4d39d8b8b507a5d_0.png)
Como se puede observar, al eliminar con cal dureza permanente debida al magnesio, se genera dureza permanente debida al calcio. La dureza permanente debida al calcio se elimina tratándola con carbonato de sodio:
![[ce]CaCl2 + Na2CO3 -> CaCO3(s) + NaCl[/ce] [ce]CaCl2 + Na2CO3 -> CaCO3(s) + NaCl[/ce]](images/latex/6d41a9b7882a407a8fd9588abc84a2f0999da5e6_0.png)
Cuando se utiliza este método para eliminar dureza en una industria, se mide la dureza total y se agrega en primera instancia cal suficiente para eliminarla y el doble de soda por si existiera magnesio. Luego se debe neutralizar el pH.
|
No falta balancear las primeras formulas químicas???
|
|
|
|
|
|
| |
    |
 |
Amintoros
Nivel 8

Registrado: 20 Mar 2008
Mensajes: 533
Carrera: Química


|
|
Sí, la única que está balanceada es la tercera, la que dice que el CaCl2 precipita 
|
|
|
|
_________________
| Elmo Lesto escribió:
|
| Bistek escribió:
|
|
por qué pasa que a veces entro al foro y esta todo en aleman?
|
Ahí aplicaron la transformada de Führer

|
cuando la yerba mate
|
|
 |
    |
 |
Palmito
Nivel 3
Edad: 32
Registrado: 27 Jul 2010
Mensajes: 52
Carrera: Industrial


|
|
| Alguien tiene resuelto el ejercicio 3 de la guía de aguas en industrial?. Porque no me sale el puntos D.
|
|
|
|
|
|
   |
    |
 |
NicoBU
Nivel 0
Registrado: 06 Feb 2012
Mensajes: 1
Ubicación: Ing. Maschwitz


|
|
| Palmito escribió:
|
|
Alguien tiene resuelto el ejercicio 3 de la guía de aguas en industrial?. Porque no me sale el puntos D.
|
Mirá, no te voy a mentir, a mi casi me da lo mismo: 24,86g de Ca(OH)2 (de 24,76) y 18,20g de Na2CO3 (de 16,16) y 16,72g de HCO3-
Siendo 5,22 g de Ca2+ y 4,34 de Mg2+:
Tenés que fijarte cuál es el limitante en la primera reacción (si tenés las fórmulas de caracciolo, a mi me da el Ca2+; te quedan entonces 0,83 g del carbonato 2(HCO3). Por esto cuando vas a eliminar el magnesio en la segunda reacción el limitante es el carbonato. Te queda entonces un remanente de magnesio que te lo sacás en la tercera, que te genera 6,88g de Ca2+, que lo eliminás con la soda Na2CO3 en la cuarta reacción.
|
|
|
|
|
|
 |
    |
 |
Palmito
Nivel 3
Edad: 32
Registrado: 27 Jul 2010
Mensajes: 52
Carrera: Industrial


|
|
ok, porque mañana rindo  y tengo varias cosas al aire. Espero que estas sean las ecuaciones(SIN BALANCEAR): y tengo varias cosas al aire. Espero que estas sean las ecuaciones(SIN BALANCEAR):
Ca(HCO3)2 + Ca(OH)2 ---> CaCO3 + H2O
Mg(HCO3)2 + Ca(OH)2 ---> CaCO3 + Mg(OH)2 + H2O
Mg(++) + Ca(OH)2 ---> Mg(OH)2 + Ca(++)
Ca(++) + Na2Co3 ---> CaCO3 + 2Na(+)
Este tema, no lo vi en clase. Aver si le pegue, hice esto. De la primera ecuacion el calcio es el límitante, saco la cantidad de bicarbonato. Sumo ambos y saco la cantidad de cal de la primera(estequiometria). En la segunda el bicarbonato es el límitante porque es lo que me quedo de la anterior, así saco la cantidad de magnesio. Sumo ambos y calculo la cantidad de cal de la segunda. Lo que me sobro de Mg lo uso en la tercera y con este saco la cal de la tercera y la cantidad de iones de calcion del producto. De ahí ya tengo la cantidad de cal. Con los iones de calcio puedo sacar la de la cuarta los gramos de soda. A menos que alguien me corrija, eso fue lo que al final entendí.
|
|
|
|
|
|
   |
    |
 |
|
|







![[ce]Ca(HCO3)2 + Ca(OH)2 -> CaCO3(s) + H2O[/ce] [ce]Ca(HCO3)2 + Ca(OH)2 -> CaCO3(s) + H2O[/ce]](images/latex/5bb297b03e7d883c1e5bcd17e235945576cf0145_0.png)
![[ce]Mg(HCO3)2 + Ca(OH)2 -> Mg(OH)2(s) + CaCO3(s) + H2O[/ce] [ce]Mg(HCO3)2 + Ca(OH)2 -> Mg(OH)2(s) + CaCO3(s) + H2O[/ce]](images/latex/038dd1cd0b0250e6cbafee14cf151eff7a9f0ff7_0.png)
![[ce]MgCl2 + Ca(OH)2 -> Mg(OH)2(s) + CaCl2(s) [/ce] [ce]MgCl2 + Ca(OH)2 -> Mg(OH)2(s) + CaCl2(s) [/ce]](images/latex/4b008606d392049c426297a6c4d39d8b8b507a5d_0.png)
![[ce]CaCl2 + Na2CO3 -> CaCO3(s) + NaCl[/ce] [ce]CaCl2 + Na2CO3 -> CaCO3(s) + NaCl[/ce]](images/latex/6d41a9b7882a407a8fd9588abc84a2f0999da5e6_0.png)


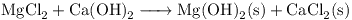



 y tengo varias cosas al aire. Espero que estas sean las ecuaciones(SIN BALANCEAR):
y tengo varias cosas al aire. Espero que estas sean las ecuaciones(SIN BALANCEAR):